1回当たりの薬価が過去最高の白血病・リンパ腫治療薬チサゲンレクルユーセルとは?
2019年5月15日の中央社会保険医療協議会で薬価が決定された白血病・リンパ腫治療薬チサゲンレクルユーセルは,1回あたりの価格が3349万3407円と超高額であることが耳目を集めました.ただ,白血病や悪性リンパ腫という病気は,有名人が罹患する時に一時的に話題になるものの,世間一般にはあまり耳にしない病名のため,これらの病気ではない方々にはそれほど関心がない情報かもしれません.しかし,血液内科医やその病気の患者さんにとっては,いよいよという思いがあるのではないでしょうか.
「チサゲンレクルユーセル」という一般名は私にも全く馴染みのない響きですが,”CAR-T(カーティー)細胞“という細胞を半人工的に製造し,患者さんに投与するという,全く新しい作用機序の抗がん剤です.
CARとは,chimeric antigen receptor(キメラ抗原受容体)の略ですが,これを見て意味が分かる人は素人ではありません.
T細胞というリンパ球(免疫の主役ともいうべき細胞)の表面には,それぞれ様々な抗原という物質を識別できる分子(受容体)がついています.ざっくり言えば,受容体が結合できる抗原に対して免疫が発動し,抗原を排除しようとします.そこで,がん細胞に特徴的な抗原を認識できる受容体に,T細胞を効率的に活性化させる分子を結合させたキメラ抗原受容体(CAR)を作るための遺伝子をT細胞に導入し,がん細胞のエキスパートであるT細胞を作ります.
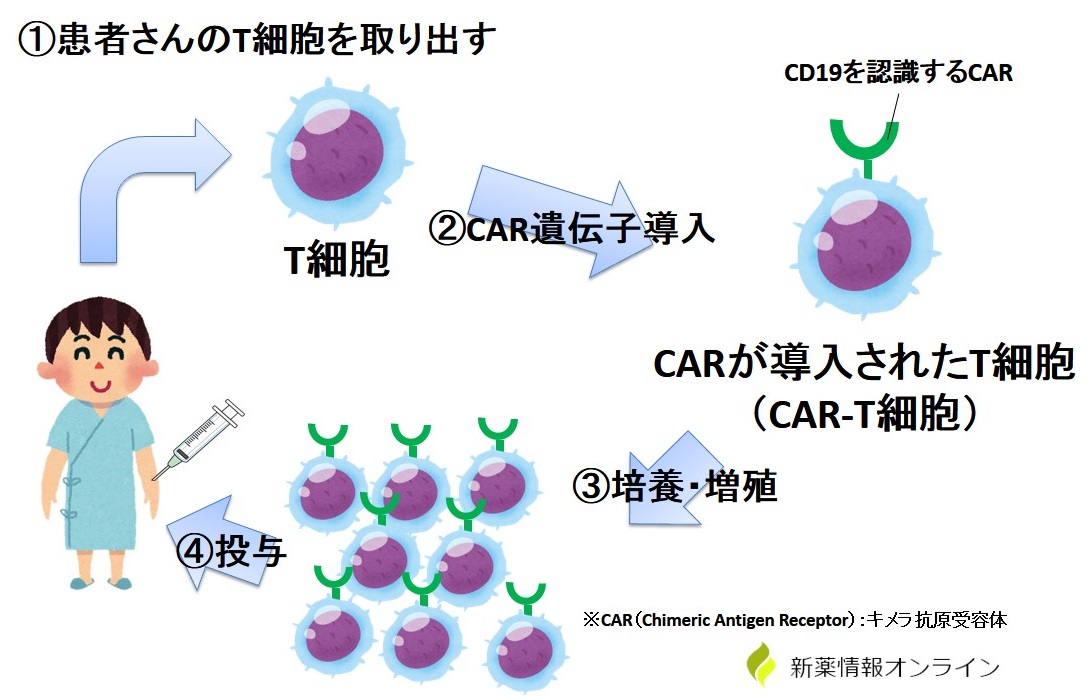
CAR-T療法とは,そのようなエキスパートT細胞を患者さんに投与して,がんの治療を行うという治療法です.
CAR-T療法は,CARが認識出来る抗原を変えれば,様々ながんの治療に応用できる可能性がありますが,今回承認されたチサゲンレクルユーセルは,”CD19″というB細胞(これもリンパ球)の代表的な表面マーカーを認識できるCARなので,B細胞系の腫瘍(非常にたくさんあります)に効果がある治療です.
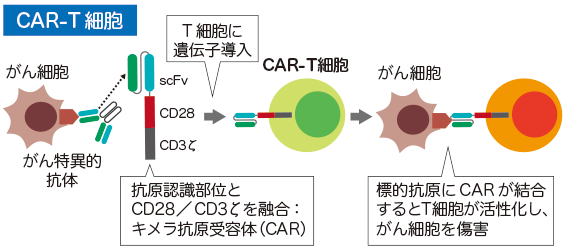
CARとは,がん細胞にだけ結合できる抗体とT細胞を活性化させるCD28/CD3ζを融合した分子である.これを患者さんのT細胞に遺伝子導入し,その改変して作られたT細胞を患者さんに投与する治療です(https://www.amed.go.jp/pr/2017_seikasyu_02-01.htmlより引用,改変).
CAR-T療法の効果
今回保険収載されたチサゲンレクルユーセル(商品名:キムリア)は,治験によって次のような効果があることが示されています.
再発難治性急性リンパ性白血病に対する効果
75人の再発難治性急性リンパ性白血病の患者に対し,チサゲンレクルユーセルを投与したところ,3ヶ月間で81%の患者が寛解になった.6ヶ月後の無イベント生存率(再発も死亡もなかった患者さんの割合)は73%,全生存率は90%で,12ヶ月後の無イベント生存率(再発も死亡もなかった患者さんの割合)は50%,全生存率は76%だった.重大な有害事象(治療のために入院を要する有害な副作用)は73%に人に起こった.サイトカイン放出症候群は77%に人に起きた.神経学的な有害事象が40%の人に起こった(N Engl J Med 2018; 378:439-448).
再発難治性びまん性大細胞型Bリンパ腫に対する効果
93人の再発難治性びまん性大細胞型Bリンパ腫の患者に対し,チサゲンレクルユーセルを投与した【研究発表時点での観察期間(チサゲンレクルユーセルを投与してから,データ収集を止めるまでの期間)の中央値は14ヶ月間】.リンパ腫が縮小する効果が得られた患者さんの割合は52%で,40%の患者さんではリンパ腫が完全に消失していた.チサゲンレクルユーセルを投与して12ヶ月時点で,無再発生存割合は65%だった.頻度が高かった重大な有害事象は,サイトカイン放出症候群(22%),神経学的異常が12%,28日以上続く血球減少が32%,感染症が20%,発熱性好中球減少症が14%だった.治療の有害事象で亡くなったと考えられる患者はいなかった(N Engl J Med 2019; 380:45-56).
CAR-T療法の重大な有害事象
サイトカイン放出症候群 (Cytokine release syndrome, CRS)
CAR-Tを輸注した後,CAR-T細胞による免疫反応(CAR-T以外によって誘発されるものもある)により,発熱や低血圧,脈が早くなるなど全身の症状が出現する有害事象です.呼吸不全になって人工呼吸が一時的に必要になるなど,かなり重篤な状態になる場合があり,集中治療室への入室が必要になることがあります.
神経学的異常
頭痛,混乱,幻覚,失語,振戦(手足の細かい震え)などの症状が起こる場合があります.
現時点でCAR-T療法を実施できる施設はない
チサゲンレクルユーセル(キムリア)は,保険収載されて薬価も決まったのですが,現時点で使用できる医療機関はありません(2019年8月26日訂正:2施設で実施可能となっています。ノバルティス社のウェブサイトの薬事法縛りのページ内に書いてある情報なので、こちらには記載しないでおきます).一般的な薬でも,製造体制が整うまで発売できないということがあります.チサゲンレクルユーセルは,医療機関で患者さん自身の細胞を採取し,それを凍結してアメリカのニュージャージー州の工場に搬送し,そこでCAR-T細胞が作られ,それが再び医療機関に運ばれて患者さんに投与されるという製造工程です.承認される医薬品の製造工程は全て管理され,品質が承認される必要があるのですが,チサゲンレクルユーセルの場合,細胞を製造する工場だけでなく,細胞を採取する医療機関も製造工程に入るため,医療機関も承認を受ける必要があるのですが,前例のない医薬品でありまだどの医療機関も承認を受けていません.医療機関で細胞処理に使われる機材や処理マニュアル,品質管理体制なども問われることになり,医療機関にとって大変な負担です.厚生労働省からの承認を受けられる施設は,かなり限られた施設になると予想されます.
承認された適応は広く,使うことができる患者さんはかなり多いと思いますが,そのような医療機関(大都市の大病院)にアクセスできる患者さんとなれば,若くて状態のいい患者さんに限られるので,高額な治療薬ですが,実際に使える患者さんは適応患者の一部になると思われます.待望のお薬ですが,実際に患者さんに投与されるのはまだまだ先になると思われます.
講義
2019年9月5日に芦屋市医師会医療センターで行われた2019年度 芦屋健康大学 第1回目講義「1回3000万円のがん治療 ー遺伝子診断とCAR-T療法について知っておくべきことー」の講義スライドを共有いたします。